ÉTUDE DE CAS
Analyse pharmacodynamique des biomarqueurs de dommages à l'ADN dans les CTC dans le cadre de l'essai de phase III BEACON dans le cancer du sein®.
Application clinique : analyse pharmacodynamique d'un agent endommageant l'ADN afin d'identifier une signature prédictive de la réponse clinique
Mots clés : CTCs , ApoStream®, pharmacodynamique, dommages à l'ADN, expression des protéines, LSC, cancer du sein
Contexte : La topoisomérase 1 est une enzyme nucléaire qui joue un rôle essentiel dans la réplication, la transcription, la recombinaison et la réparation de l'ADN. Il s'agit d'une cible médicamenteuse courante en oncologie. L'un de ces agents thérapeutiques, l'étirinotécan pégol (NKTR-102), est un inhibiteur unique de la topoisomérase 1 à longue durée d'action, conçu pour une exposition prolongée des cellules tumorales ; son métabolite actif, le SN38, stabilise le complexe de la topoisomérase 1, ce qui entraîne des cassures double brin de l'ADN et, finalement, l'apoptose.
L'étude BEACON de phase 3, ouverte, randomisée et multicentrique, compare le NKTR-102 au traitement choisi par le médecin (TPC) chez des patientes atteintes d'un cancer du sein localement récurrent ou métastatique, précédemment traitées par une anthracycline, un taxane et de la capécitabine, et examine les effets pharmacodynamiques sur les biomarqueurs de dommages à l'ADN lors d'un traitement par le NKTR-102.
Méthodes : ApoCell a d'abord développé et qualifié un test de biomarqueur multiplexé pour la détection de six biomarqueurs différents - Topoisomérases 1 et 2, γH2AX (un marqueur de dommages à l'ADN double brin), RAD51 (un membre de la machinerie de réparation des dommages à l'ADN double brin), Ki-67 (un membre de la machinerie de réparation des dommages à l'ADN double brin).
), Ki-67 (marqueur de prolifération) et ABCG2 (transporteur d'efflux pour le SN38) - dans les CTC par cytométrie à balayage laser (LSC).
Du sang a ensuite été prélevé chez tous les patients participant à l'étude à quatre moments différents, comme le montre la figure 1.
Tous les échantillons ont été enrichis en CTC par ApoStream® ; les cellules enrichies ont été cytospunies sur des lames et colorées avec les six biomarqueurs d'intérêt et les marqueurs phénotypiques des CTC (cytokératine, CD45 et DAPI).
Les CTC ont été identifiées comme des cellules DAPI+/CK+/CD45-, et le niveau d'expression de chaque marqueur a été examiné dans ces cellules. En outre, l'apoptose a été mesurée dans les CTC isolées à l'aide du TUNEL.
Résultats :

Figure 1 : Calendrier du traitement et de l'analyse des biomarqueurs. Calendrier du traitement et de l'analyse des biomarqueurs. Les CTC ont été prélevées à C1D1, C2D1, C4D1 et à la fin du traitement pour l'analyse des biomarqueurs spécifiques à la cible dans les CTC.
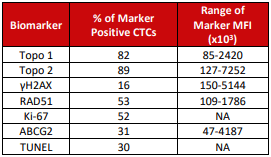
Des CTC ont été détectées dans 93% des échantillons pré-dosés (médiane : 217 ; intervalle : 7-15000 cellules). Les biomarqueurs ont été exprimés dans des gammes et des intensités variables dans tous les échantillons.
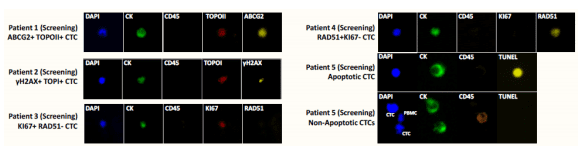
Impact : ApoCell a conçu et qualifié avec succès un test pour la détection simultanée de multiples biomarqueurs de dommages à l'ADN en réponse à une thérapie, et a incorporé avec succès ce test dans une étude clinique de phase III.
Ce test a été intégré avec succès dans une étude clinique de phase III. L'étude BEACON indique qu'ApoStream® est capable d'isoler les CTC d'une majorité de patients et représente un moyen moins invasif d'obtenir des données biologiquement significatives pour éclairer les décisions thérapeutiques. Les biomarqueurs pharmacodynamiques peuvent être mesurés de manière fiable dans les CTC et peuvent constituer une mesure prédictive potentielle de la réponse clinique.
mesure prédictive potentielle de la réponse clinique.
Références : 1. Hoch U, et al. "Etirinotecan Pegol Target-Specific Pharmacodynamic Biomarkers Measured in Circulating Tumor Cells (CTCs) ApoCell, Inc. from Patients in the Phase III BEACON Study in Patients with Metastatic Breast Cancer (mBC)." ASCO 2014.