ÉTUDE DE CAS
Validation d'une méthode LSC pour la mesure de γH2AX dans les cellules mononucléaires du sang périphérique humain
Application clinique : surveillance de l'étendue des lésions de l'ADN en réponse à la chimiothérapie
Mots clés : développement d'un test , γH2AX, dommages à l'ADN, PBMC
Contexte : De nombreux agents chimiothérapeutiques sont conçus pour inhiber la croissance ou induire l'apoptose des cellules malignes en provoquant des lésions de l'ADN. Le topotécan, un inhibiteur des isomérases de l'ADN, s'intercale entre les bases de l'ADN et provoque des cassures double brin (CDB), et l'absence de réparation de l'ADN entraîne la mort cellulaire apoptotique. La phosphorylation de l'histone H2AX sur la sérine 129 (γH2AX) se produit sur les sites entourant les cassures double brin de l'ADN et peut fournir une mesure du nombre de cassures double brin dans une cellule. Pour surveiller l'étendue des dommages à l'ADN et, en fin de compte, l'efficacité du topotécan ou d'autres agents similaires, ApoCell a développé un test de biomarqueur pour la détection des niveaux d'expression de la γH2AX.
Méthodes : Le sang de donneurs sains a été traité ex vivo avec du topotécan. Plusieurs sous-types cellulaires ont été examinés (CD3+, CD4+, CD14+, CD15+, CD16b+, CD19+, CD20+, CD33+, CD34+, CD45+, CD133+) à l'aide de la cytométrie à balayage laser (LSC) afin d'identifier les sous-populations présentant la plus forte induction de γH2AX en réponse au traitement. Les trois sous-types présentant la plus forte induction de γH2AX ont ensuite fait l'objet d'une analyse plus poussée afin de déterminer une relation dose-réponse. L'essai a été transféré dans une autre installation, où une formation et une validation croisée ont été effectuées pour démontrer la reproductibilité des résultats.
Résultats : le criblage initial des phénotypes cellulaires a montré des résultats mitigés dans l'induction de γH2AX en réponse au traitement par topotécan. Les phénotypes qui présentaient les réponses les plus cohérentes étaient CD3+, CD14+ et CD16b+. Ces trois phénotypes ont été examinés plus en détail chez deux donneurs distincts après un traitement de deux heures à deux concentrations de topotécan, comme le montre la figure 1 ci-dessous. L'étalonnage croisé des instruments LSC sur les deux sites d'essai a été effectué pour déterminer les paramètres de balayage équivalents, puis les effets du traitement avec un agent endommageant l'ADN sur une lignée cellulaire ont été comparés sur les deux sites, comme on peut le voir sur la figure 2.
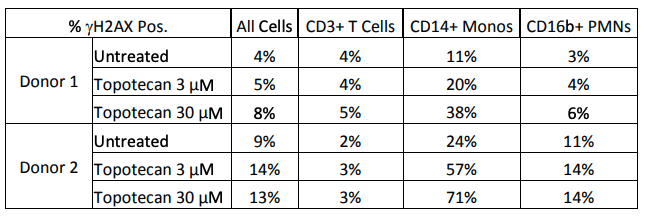
Figure 1 : Effets du traitement au topotécan sur le nombre de cellules γH2AX+. Effets du traitement par le topotécan sur le nombre de cellules γH2AX+ Les effets du traitement par le topotécan ont été examinés sur trois phénotypes cellulaires chez deux donneurs. Un traitement de deux heures aux concentrations ci-dessus n'a pas induit d'augmentation des lymphocytes T CD3+, des PMN CD16b+ ou de la population de tous les PBMCs lorsqu'ils sont considérés dans leur ensemble ; cependant, une augmentation dose-dépendante claire a été observée chez les deux donneurs dans les monocytes CD14+.

Figure 2 : Résultats de la validation croisée de la méthode LSC sur ApoCell et NCI. Résultats de la validation croisée de la méthode LSC sur ApoCell et NCI Après avoir optimisé les paramètres de balayage entre les deux sites, les cellules NCI-H460 ont été traitées avec de la gemcitabine, un autre agent endommageant l'ADN. Les cellules traitées ont été comparées aux cellules non traitées sur les deux sites en ce qui concerne l'intensité de la coloration γH2AX et le pourcentage de cellules positives. La tendance sur les deux sites illustre une induction de γH2AX après le traitement.
Impact : ApoCell a développé un test fiable pour la détection de γH2AX dans différents sous-types cellulaires du sang humain. Le test a été transféré avec succès à d'autres laboratoires.
Références : 1. Davis, D.W., et al. "Sensitive Detection of Gamma-H2AX Induction as a Pharmacodynamic Marker for Profiling Patients Treated with Topotecan". ASCO, 2010.